«El oxígeno es un veneno lento» – Joseph Priestley.
Imagina abrir tu armario y oler aceite rancio que huele a cartón mojado, o una manzana que se oscurece en minutos. Mientras algunos alimentos como la miel parecen eternos, la mayoría esconde reacciones químicas silenciosas que los arruinan rápido. ¿Por qué sucede esto y cómo evitarlo?
A continuación, exploramos qué sucede realmente dentro de tus alimentos, cómo estos cambios afectan tu comida… y qué tan peligroso puede ser ignorarlo.
¿Por Qué Caducan los Alimentos? La Base Química.
Todos los alimentos perecederos caducan por reacciones químicas naturales: oxidación (ataque del oxígeno), hidrólisis (acción del agua) y acción enzimática (proteínas internas que se activan). Estas alteran sabor, olor, textura y nutrientes, incluso sin bacterias. A diferencia de los «inmortales» del artículo anterior (baja humedad y estabilidad), estos tienen agua y compuestos reactivos que invitan al deterioro .
Oxidación: cómo el oxígeno degrada grasas y aceites.
La oxidación ocurre cuando el oxígeno del aire rompe los enlaces de los ácidos grasos insaturados, presentes en alimentos como aceite de oliva, girasol, coco, aguacate, frutos secos o mantequilla. Primero se forman peróxidos inestables y, con el tiempo, aldehídos como hexanal (olor a hierba vieja) o (E)-2-hexenal (olor a cartón rancio), responsables del mal sabor y aroma. Factores como luz, calor o metales como hierro aceleran esta reacción, y la hidrólisis puede agravar el deterioro al liberar ácidos grasos libres.
En alimentos concretos:
- Aguacate: su pulpa se vuelve marrón al exponerse al aire por oxidación enzimática (polifenoloxidasa). Esto no indica que esté dañado; sigue siendo comestible, aunque el sabor puede volverse más amargo. Solo cuando aparecen manchas negras profundas, mal olor o moho, se considera deteriorado.
- Aceites vegetales: al enranciarse desarrollan olores desagradables y pierden calidad, especialmente si se reutilizan o se almacenan mal.
- Frutos secos y mantequilla: pueden adquirir sabor rancio por la combinación de oxidación e hidrólisis.
En pocas palabras, la oxidación es una reacción química que afecta principalmente el sabor, aroma y apariencia, pero no siempre significa que el alimento sea dañino.
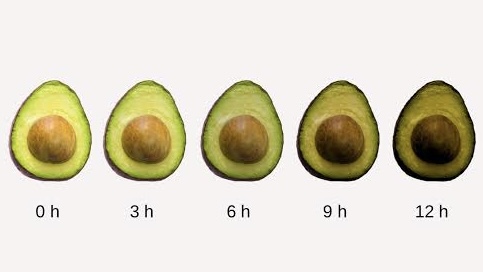
Aguacate en buen estado: pulpa verde, suave y cremosa, con aroma delicado. Al exponerse al aire, se oxida (por efecto de la polifenoloxidasa) y se vuelve marrón, pero sigue siendo comestible, aunque con posible sabor más amargo. Si presenta manchas negras profundas, mal olor o moho, está deteriorado.
Reacción de Maillard: Del Sabor Tostado al Peligro.
La reacción de Maillard ocurre cuando azúcares simples reaccionan con aminoácidos al calentar alimentos (frituras, asados, panes), formando melanoidinas que dan color y sabor. En exceso genera acrilamida, un posible carcinógeno, y reduce vitaminas sensibles al calor, como C y E. Se observa en carnes grilladas, papas fritas y dulces caramelizados.
Explicación clara: Piensa en dorar cebolla: sabroso al inicio, pero quemado genera compuestos amargos y dañinos. Tiempo y temperatura alta lo empeoran, bajando la digestión de proteínas.
Enzimas: Los Saboteadores Internos de Frutas y Verduras.
En frutas cortadas como manzanas, mangos, bananas o aguacates, la enzima polifenol oxidasa (PPO) oxida polifenoles, formando melaninas pardas en pocos minutos. Verduras como patatas reaccionan de manera similar. Ácidos como limón o vinagre pueden retrasar esta oxidación al donar electrones y neutralizar la enzima.

Cuando cortas una manzana, la polifenol oxidasa (PPO) de la fruta oxida sus polifenoles, formando melaninas pardas en minutos. Este cambio de color es solo visual: la manzana sigue siendo comestible.
Simultáneamente, las vitaminas también sufren degradación: la vitamina C (ácido ascórbico ) se oxida a dehidroascórbico por acción de luz o calor, perdiendo hasta 30-50 % en pocos días en alimentos como naranjas, kiwis o pimientos. Las vitaminas liposolubles A y E se degradan con la exposición al oxígeno.
En conjunto, estos procesos muestran que el color marrón o la pérdida de nutrientes son consecuencia de reacciones químicas naturales, pero no siempre indican que el alimento sea dañino; algunas alteraciones afectan solo apariencia o valor nutricional.
Fechas en Etiquetas: Seguridad vs. Calidad.
- Caducidad: Riesgo microbiológico real en alta humedad (aw >0.85) y pH neutro, como carnes, leche o huevos. Descartar sí o sí.
- Consumir preferentemente: Calidad óptima; oxidación o Maillard ya empezaron, pero seguro (aceites, galletas).
- Lote: Para rastreo químico en conservas.
|
Tipo de Fecha |
Qué Indica Químicamente |
Ejemplos |
|
Caducidad |
Bacterias por aw alta |
Leche, pescado fresco |
|
Preferente |
Oxidación/Maillard |
Aceites, panes envasados |
|
Lote |
Trazabilidad |
Latas de atún, frijoles |
Algunas curiosidades.
- Snacks “eternos” gracias al nitrógeno: Muchos snacks fritos y alimentos secos se envasan con nitrógeno, que desplaza el oxígeno para reducir la oxidación y prolongar la frescura. Esto evita rancidez, aunque la reacción de Maillard aún puede generar acrilamida.
- Rancidez universal: hexanal como marcador: Durante la oxidación de grasas, se forman compuestos secundarios como hexanal, responsables del olor a “hierba vieja” o cartón rancio, presentes en aceites de coco, oliva y otros frutos secos. Fuente
- Frutas que se oxidan en segundos: Manzanas, mangos y otras frutas se vuelven marrones rápidamente por la acción de la enzima polifenol oxidasa (PPO). El jugo de limón puede ralentizar esta reacción, “congelando químicamente” el color y sabor.
- Vitamina C sensible a luz y oxidación: La vitamina C (ácido ascórbico) se degrada rápidamente con la exposición a luz UV y oxígeno, reduciendo hasta 30-50 % su contenido en jugos de naranja, guayaba y otros alimentos frescos.
Trucos Prácticos para Frenar la Química.
- Refrigera los perecederos: mantenerlos a baja temperatura ralentiza la acción de enzimas y bacterias.
- Usa envases opacos y herméticos: bloquean la luz y el oxígeno, protegiendo sabor, color y nutrientes.
- Evita calor y humedad extremos: cambios bruscos aceleran la degradación; congela grasas para detener la oxidación.
Y dicho todo lo anterior, y tomando en cuenta que estamos a las puertas de Semana santa, desearte no sólo unas felices fiestas (en caso de que las célebres), sino también que este post te haya servido para entender mejor la química detrás de tus comidas favoritas y cómo mantenerlas en su mejor estado más tiempo.
Sin más que añadir, gracias por leerme, y… ¡Hasta la próxima!

