“Para cada problema complejo hay una solución que es simple, clara… y equivocada.”- H. L. Mencken.
Hay ideas que, sobre el papel, resultan difíciles de cuestionar. Planteamientos que prometen mejorar el entorno, reducir emisiones o corregir desequilibrios, y que por eso mismo se aceptan casi de forma automática.
Sin embargo, cuando se llevan a la práctica, la perspectiva cambia. Ya no se trata solo de si funcionan, sino de cómo lo hacen, qué implican y qué efectos pueden generar más allá del objetivo inicial.
Aquí entra en juego una línea de trabajo poco conocida fuera del ámbito científico, aunque no es nueva. Una intervención aparentemente sencilla, basada en una reacción química conocida, que plantea una forma directa de actuar frente a un problema global.
¿Qué se hizo exactamente?
En Agosto de 2025, concretamente el día 13, un equipo del Woods Hole Oceanographic Institution llevó a cabo un ensayo en el Golfo de Maine (EE.UU) como parte del proyecto LOC-NESS.
En total, se liberaron alrededor de 65.000 litros de solución de hidróxido de sodio (NaOH) en una zona concreta del océano. La operación se realizó de forma controlada a lo largo de unas seis horas, en lugar de tratarse de un vertido continuo durante varios días.
Para poder seguir la dispersión de la mezcla, se utilizó además un colorante visible, lo que permitió observar cómo se diluía en el agua.

Zona del Golfo de Maine durante el experimento, donde el colorante permitió seguir la dispersión de la solución alcalina en el agua.
La imagen es llamativa. El agua se tiñe y permite seguir el recorrido de la mezcla en el océano.
A partir de ese momento, el experimento continuó durante los días siguientes con el seguimiento de la dispersión, los cambios de pH y la evolución química del sistema. El vertido fue puntual, pero la observación se extendió en el tiempo.
Se trató, además, de un ensayo a pequeña escala, limitado y cuidadosamente controlado, diseñado precisamente para evaluar su comportamiento en condiciones reales antes de considerar posibles aplicaciones más amplias.
Aunque se llevó a cabo en 2025, los resultados no se difundieron de forma inmediata. Como ocurre habitualmente en investigación científica, los datos se analizan, se contrastan y se presentan primero en entornos especializados.
Los primeros resultados se dieron a conocer en 2026 en foros como el Ocean Sciences Meeting, lo que explica que este experimento haya empezado a aparecer recientemente en análisis y publicaciones.
La base científica.
El planteamiento tiene fundamento. Forma parte de una línea de investigación conocida como aumento de alcalinidad oceánica, estudiada por organismos como la NOAA.
Cuando el hidróxido de sodio se disuelve en agua:
NaOH ⇌ Na⁺ + OH⁻
El ion hidróxido eleva el pH, haciendo el medio más alcalino. Esto modifica el equilibrio del carbono disuelto:
CO₂ + H₂O ⇌ H₂CO₃ ⇌ HCO₃⁻ + H⁺ ⇌ CO₃²⁻ + H⁺
En este equilibrio, el CO₂ disuelto en el agua no permanece como gas, sino que se transforma en otras especies químicas como bicarbonato y carbonato. La liberación de iones H⁺ está directamente relacionada con la acidez del agua, de modo que cualquier cambio en el pH altera este sistema.
Cuando el pH aumenta, el equilibrio se desplaza hacia estas formas más estables, lo que en teoría facilita la absorción de CO₂ desde la atmósfera.
¿Qué se logró en la práctica?
Los datos disponibles muestran un aumento medible del pH del agua de mar, pasando aproximadamente de valores cercanos a 7,9 a 8,3. Se trata de un cambio relevante desde el punto de vista químico, ya que sitúa el agua en rangos comparables a los niveles preindustriales.
Sin embargo, este efecto fue localizado y temporal. El océano tiene una enorme capacidad de dilución, lo que hace que la alcalinidad añadida se disperse rápidamente y limite su alcance.
En cuanto a la captura de CO₂, las estimaciones iniciales apuntan a cifras en torno a 10 toneladas.
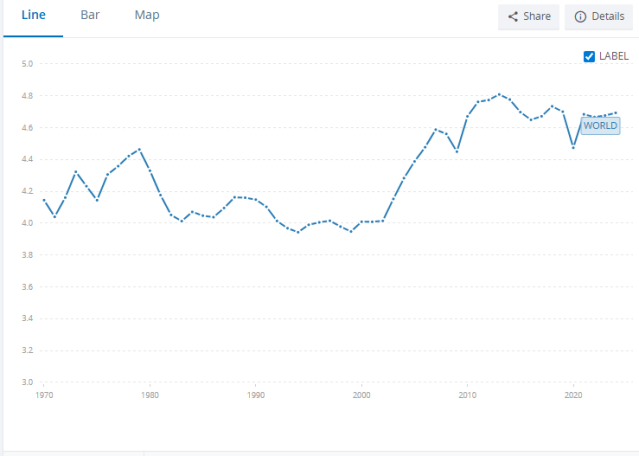
Evolución de las emisiones globales de CO₂ desde 1970, que permite contextualizar la escala del problema frente a intervenciones puntuales. Fuente: EDGAR (JRC, Comisión Europea) e IEA. Los datos más recientes disponibles corresponden a 2024. Este desfase es habitual en este tipo de estadísticas, ya que las emisiones deben recopilarse, verificarse y armonizarse antes de su publicación.
En este contexto, conviene aclarar qué significa realmente ese dato.
Cuando se habla de CO₂ capturado, se hace referencia al dióxido de carbono que deja de estar en la atmósfera y pasa a disolverse en el océano en forma de bicarbonato y carbonato, dentro del sistema químico del agua.
Para ponerlo en perspectiva, una persona en un país industrializado emite aproximadamente entre 6 y 10 toneladas de CO₂ al año, en línea con los datos recogidos por el World Bank.
Estas emisiones proceden principalmente de la quema de combustibles fósiles en sectores como el transporte, la generación de energía, la industria o la calefacción.
Si se toma como referencia el transporte, un coche medio puede emitir en torno a 2 a 2,5 toneladas de CO₂ al año, dependiendo del uso.
Esto permite dimensionar mejor el resultado del experimento: la cantidad de CO₂ capturada equivale aproximadamente a las emisiones anuales de una sola persona o a varios vehículos en circulación durante un año.
En ese sentido, el ensayo resulta interesante desde el punto de vista científico, pero su impacto sigue siendo limitado si se compara con la escala global de emisiones.
Implicaciones que no se ven.
El hidróxido de sodio es un compuesto altamente alcalino, utilizado en procesos industriales y productos de limpieza. En contacto directo puede provocar daños en tejidos biológicos.
En el entorno marino, un aumento localizado del pH puede afectar a organismos sensibles, especialmente a aquellos que dependen de un equilibrio químico muy concreto para funciones como la calcificación, la respiración o la regulación interna.
Además, modificar el pH no solo cambia la acidez del agua, sino también la disponibilidad de distintas especies químicas, lo que puede alterar procesos biogeoquímicos clave.
También pueden producirse reacciones secundarias que reduzcan la eficiencia del proceso, como la formación de carbonato cálcico:
Ca²⁺ + CO₃²⁻ ⇌ CaCO₃ (s)
En este caso, parte del carbono capturado puede acabar formando sólidos, lo que limita su papel dentro del sistema de equilibrio del carbono disuelto.
Este tipo de efectos forma parte de las cuestiones que siguen siendo objeto de estudio, especialmente en lo que respecta a su posible impacto a mayor escala.
Cuando la solución es más simple que el sistema.
El interés de este experimento no está solo en el resultado: está en lo que representa. Porque no es un caso aislado.
En distintos ámbitos aparecen soluciones que parecen lógicas en un contexto concreto, pero que al aplicarse sobre sistemas complejos generan efectos que no siempre se anticipan.
La energía eólica, por ejemplo, es una herramienta clave en la transición energética. Sin embargo, organismos como el U.S. Fish & Wildlife Service han documentado que los aerogeneradores pueden afectar a aves y murciélagos en determinadas ubicaciones, tanto por colisiones como por alteraciones del hábitat y del comportamiento.
En la misma línea, el U.S. Geological Survey señala que estos efectos dependen en gran medida de factores como la localización, las rutas migratorias o la densidad de instalaciones.
Algo similar ocurre con la expansión de grandes instalaciones solares. Organismos como la International Energy Agency han señalado la necesidad de evaluar cuidadosamente su impacto sobre el uso del suelo, ya que en algunos casos implica la transformación de grandes superficies de terreno, incluyendo la alteración de ecosistemas y procesos de deforestación.

La transición energética plantea soluciones necesarias, pero también introduce nuevos desafíos cuando se analiza su impacto a gran escala.
Teniendo en cuenta todo lo anterior, se puede afirmar que el experimento deja de ser solo una reacción química y pasa a plantear una cuestión más amplia.
Una solución puede parecer sostenible en teoría, pero la pregunta cambia cuando su aplicación implica intervenir sobre un sistema complejo sin comprender completamente sus efectos.
La base científica puede ser sólida. La intención también. Pero entre una idea que funciona en condiciones controladas y una solución viable a escala real hay una diferencia importante. Entender esa diferencia es, probablemente, lo más relevante de todo.
Para cerrar, cabe preguntarse: ¿todo vale cuando se plantea como una solución para el medio ambiente?
Sin más que añadir, gracias por leerme, y… ¡hasta la próxima!
